INTRODUÇÃOA Síndrome de Goldenhar é uma herança multifatorial, apresentando manifestações mais severas quando esta herança é paterna, autossômica dominante. Também pode ser identificada pelas sinonímias displasia óculo-aurículovertebral, displasia OAV, seqüência fascioauricolovertebral, seqüência FAV, espectro oculoauriculovertebral.
Esta patologia tem como tríade clássica as alterações oculares, auriculares e vertebrais, podendo apresentar sinais sistemáticos, com anomalias cardíacas, renais e de sistema nervoso central (1, 2, 3, 4, 5). Ocorre a partir de uma disrupção vascular no embrião, entre o 35º e 40º dia de gestação, impedindo a morfogênese correta das estruturas derivadas do primeiro e segundo arcos branquiais, resultando no quadro clínico presente ao nascimento (2).
Esta doença é reconhecida como uma síndrome porque, além da disostose mandibulofacial, existe a presença adicional de anomalias vertebrais e dermóides epibulbares (6). A incidência é de um para cada 56.000 nascimentos (7), predominando em homens e na forma bilateral, podendo associar-se a transtornos genéticos, cromossômicos e teratogênicos ambientais. Na Irlanda do Norte a taxa de prevalência é de um para cada 45.000 nascidos vivos (8). Já foram relatados casos familiares com herança autossômica dominante com expressividade variável, além de casos de consanguinidade entre os pais, sugerindo herança autossômica recessiva. Microssomia hemifacial e as displasias de pavilhão auricular estão presentes em 65% dos casos, tumores epibulbares e as cardiopatias congênitas em 50% dos casos, sendo a Tetralogia de Fallot a mais freqüente (9). Até 30% dos pacientes apresentam alterações de coluna, variando desde espinha bífida e hemivertebra até fusão e hipoplasia vertebral. Em 5% ocorrem alterações renais e de traquéia. Estima-se que 5% a 10% tenham algum grau de deficiência mental, com ou sem alteração estrutural do sistema nervoso central.
Nesta síndrome ocorre um complexo sintomático congênito de etiologia desconhecida, no qual as principais alterações estão localizadas no olho (dermóide e/ou lipodermóide epibulbar), na orelha externa (apêndices auriculares, fístulas cegas) e na coluna vertebral (hemivértebras, fusões vertebrais e outras malformações diversas), estando também associada a outras malformações congênitas viscerais ou faciais envolvendo estruturas derivadas do 1º e 2º arcos branquiais (10). É causada por herança multifatorial, tendo geralmente alterações unilaterais em um mesmo desenvolvimento contínuo (1). Quando bilateral, um dos lados é mais afetado (2).
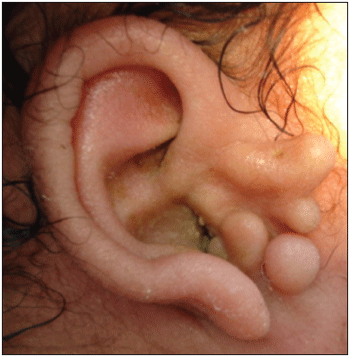
Figura 1. Síndrome de Goldenhar - Displasia de pavilhão auricular direito, com presença de apêndices pré-auriculares.
O diagnóstico da Síndrome de Goldenhar não deve basear-se somente em resultados radiológicos ou laboratoriais. Deve ser baseado em aspectos clínicos e associados com condições sistêmicas de nascimento e achados radiológicos (11).
A estratégia terapêutica está diretamente relacionada com o tipo de acometimento, uni ou bilateral, podendo assim abrir mão de procedimentos cirúrgicos ou outros métodos específicos (12).
Motivou-nos ao estudo mais profundo das anomalias congênitas, dentre elas a Síndrome de Goldenhar, a atuação interdisciplinar presente no dia-a-dia do Hospital Universitário Bettina Ferro de Souza, entre os Serviço de Otorrinolaringologia, Oftalmologia, Pediatria, Psicologia, Serviço Social e Fisioterapia, sobretudo no que se refere a assistência à crianças portadoras de diversas necessidades especiais. Justifica-se a realização deste trabalho pela necessidade de alertar os profissionais de saúde para a ocorrência desta síndrome, pouco freqüente, mas com graves conseqüências aos seus portadores, sobretudo quando expostos a um diagnóstico tardio. O tema é amplamente estudado no banco de dados gratuito Online Mendelian Inheritance in Man - OMIM, o qual traz informações e artigos constantemente atualizados (13).
REVISÃO DA LITERATURA EtiopatogeniaA etiopatogenia multifatorial inclui fatores nutricionais e ambientais que resultam em distúrbios de blastogênese. Não existem informações para identificar estes fatores etiológicos (14). Verificaram-se anormalidades cromossômicas e teorias sugerem um distúrbio da parte superior de células neurais como a causa da doença. A influência de outros fatores, incluindo o meio ambiente, durante a gravidez pode ser responsável pelo surgimento da doença. A ingestão de algumas drogas como a cocaína, talidomida, ácido retinóico e tamoxifen pela mãe são relatados como fatores para o desenvolvimento da doença.
Apesar de terem sido descritos casos novos com herança autossômica dominante, acredita-se que a grande maioria é esporádica. Por outro lado, as anomalias do 1º e 2º arcos branquiais têm sido observadas em crianças nascidas de mães expostas à talidomida, primidona e ácido retinóico, além de mães diabéticas (15, 16). Embriologicamente, o defeito oculo-auriculo-vertebral tem sido considerado uma anomalia do 1º arco branquial, mas essa alteração não explica as anomalias no cérebro, coração, rins ou espinha dorsal (17).
Verificou-se importante associação entre o desenvolvimento dessa síndrome e a presença de malnutrição, contato com tabaco e herbicida, os quais levam à produção de radicais livres que provocam a quebra do DNA resultando em malformação congênita.
Manifestações ClínicasA tríade clássica característica desta síndrome é formada por alterações oculares, auriculares e vertebrais (18). Podem estar associados: hipoplasia malar e/ou mandibular; hipoplasia da musculatura facial; micrognatia; apêndices pré-auriculares e displasia de orelha externa; hemivértebra ou hipoplasia de vértebras cervicais, torácicas ou lombares; dermóides epibulbares; microftalmia; palato e/ou lábio fendido; anomalias cardíacas; anomalias renais e de sistema nervoso central. Entretanto, devido à variabilidade de quadro clínico, há pacientes acometidos com manifestações clínicas mínimas predominando assimetria facial e as displasias de pavilhão auricular.
Podem ser encontradas protuberâncias ou fistulas pré-auriculares como primeira manifestação, seguidas das alterações ortopédicas. As anormalidades esqueléticas mais encontradas são de vértebras cervicais, como occipitalização do Atlas, sinostoses, vértebras cuneiformes, sendo de grande incidência o acometimento de vértebras mais inferiores, a semelhança do que ocorre na espinha bífida. Outro comprometimento freqüente são os oculares, como a alteração do dermóide epibulbar.
Também foram encontrados dados de descrição post-mortem de pacientes com 1 a 2 anos, onde verificou-se a ausência do forame olfatório na lâmina crivosa do osso etmóide e ipsilateral do bulbo e trato olfatório.
Há importante associação com alterações cardíacas, pulmonares e renais evidenciadas predominantemente nos primeiros meses de vida, mas há relatos de diagnósticos em pacientes adultos com mais de trinta anos de idade. Foram descritos acometimentos raros como lipoma de corpo caloso (1).
Segundo os achados genéticos, as manifestações são em geral, mais graves quando a herança é paterna, autossômica dominante, podendo aparecer, inclusive, evidencias de heterogeneidade genética. Os pacientes apresentam maior susceptibilidade para diabetes, hiperlipidemia e para os efeitos embriopatológicos causados pela rubéola. Algumas alterações estruturais do osso temporal facilitam, individualmente, a ocorrência de meningite e comprometimento posterior das orelhas.
As malformações auriculares podem ser unilaterais ou bilaterais, surgindo umbilicação do pavilhão, o qual pode implantar-se anteriormente ou inferiormente, além de sua forma variar da micrognatia, até o alargamento do lóbulo ou mesmo anognatia. Em alguns casos pode coexistir com fistulas periauriculares. O conduto auditivo externo pode apresentar-se com estenose, agenesia ou ter o conduto auditivo terminando em fundo de saco. São observadas também mastoidites.
Quando feita a exploração da cavidade oral, verificam-se as características do palato, cujas alterações nos mostram relação com possíveis transtornos da tuba auditiva e da ventilação da orelha média.
São observadas as características de implantação do cabelo, das sobrancelhas, olhos, nariz e pescoço revelando associação com síndromes disgenéticas (19).
Muitos pacientes foram relatados apresentando anomalias complexas multisistêmicas, associadas à síndome de Goldenhar, incluindo problemas respiratórios, dermatológicos, ósseos, genitourinários, gastrointestinais, do sistema nervoso central, muscular e do sistema endócrino (20). A frequência das malformações cardiovasculares na síndrome de Goldenhar varia de 5% a 58%. A principal razão para essa variação é a adoção de diferentes critérios diagnósticos. Problemas cardíacos congênitos e tetralogia de Fallot são as malformações cadíacas mais encontradas nessa síndrome. Outros problemas cardiovasculares relatados incluem coarctação da aorta, malformação de ductos arteriais, transporte dentro de importantes artérias, destrocardia, defeitos septais atrial e ventricular, anomalias de artérias coronárias, descência de aorta para o lado direito, anomalias das veias cavas superior e inferior e distúrbios arrítmicos semelhante ao que acontece na síndrome de Wolff-Parkinson-White (21).
Diagnóstico e Exames ComplementaresAtualmente, este diagnóstico pode ser estabelecido desde o pré-natal. Estudo recente detectou anomalias congênitas múltiplas em achados ultrassonográficos em 20 casos. A idade gestacional no diagnóstico variou de 15 a 35 semanas e em mais da metade dos casos estava associado a oligohidramnio ou polihidramnio. As características observados foram: malformações faciais presentes em 52% dos casos, como microftalmia, anormalidades auriculares, assimetria facial e fenda facial; dentre as alerações neurológicas observou-se hidrocefalia, encefalocele occiptal e hipoplasia cerebelar, ocorridas em 47% dos achados; defeitos cardíacos, aplasia radial e agenesia renal foram vistos em menos ocorrência (9,22).
Quanto ao diagnóstico pós-natal, há um consenso global que o diagnóstico da Síndrome de Goldenhar não deve ser baseado somente em resultados radiológicos ou laboratoriais, mas considerar os aspectos clínicos e associados com condições sistêmicas de nascimento e achados radiológicos (11). A maioria dos autores consideram a presença de anomalias das orelhas (microtia) e de apêndices na orelha necessários para diagnóstico. Além disso, assimetria facial , hipoplasia facial e /ou mandibular, tumor dermóide epbulbar, alterações palpebrais, anomalias vertebrais, fissura facial lateral e problemas renais também são observados (23,24).
Tanto testes laboratoriais, quanto de imagem são importantes para o diagnóstico por estarem diretamente relacionados as alterações provocadas. A radiografia dos ossos do zigomático mostra uma deficiência macroscópica de desenvolvimento da simetria óssea. Também existe uma possibilidade de agenesia desses ossos, com defeito de fusão do arco zigomático e agenesia dos ossos palatinos. Fenda palatina deve ser observada radiograficamente. Exames oftalmológicos e otorrinolaringológicos também são importantes para o diagnóstico final (25).
A avaliação audiológica compreende a Audiometria Tonal Limiar, Imitanciometria, Potencial Evocado Auditivo de Tronco Encefálico (BERA) e Emissões Otoacústicas Evocadas Transientes e Produto de Distorção.
É necessário realizar o exame funcional da audição para uma detecção precoce das malformações, tanto unilaterais como bilaterais. Observa-se principalmente hipoacusia condutiva entre 50 dB e 70 dB, podendo coexistir com malformação da orelha interna, traduzidas em hipoacusias mistas, com perdas auditivas entre 80 dB e 90 dB.
O exame radiológico de escolha é a tomografia computadorizada da mastóide, que nos informa sobre o estado das orelhas médias e internas e sobre o estado de pneumatização das mastóides. Estes exames devem ser realizados após os três anos. É importante a realização de estudos genéticos e descartar malformações em outros sistemas (26).
Diagnóstico diferencialEm razão da heterogeneidade clínica, é importante atentar para outras possibilidades diagnósticas, como as associações com as síndromes de Townes-Brocks e branquiooto-renal. O diagnóstico diferencial com essas outras entidades é feito com base no padrão das anomalias encontradas (27).
Quando há malformações cardiovasculares e/ou sintomatologia que indique problema cardíaco associado ou não a outras características clássicas da síndrome de Goldenhar, é necessário fazer diagnostico diferencial com outros problemas genéticos que apresentam achados semelhantes como Síndrome de Willians, Síndrome de Ehlers-Danlos e Doença de Fabry (28).
TratamentoQuanto as alterações auriculares, o emprego da estratégia terapêutica correta deve considerar se a malformação é unilateral ou bilateral e se apresenta associação com outra síndrome digenética.
No caso da alteração ser unilateral recomenda-se fazer a cirurgia a partir dos cinco anos, sendo esta realizada em dois momentos, o primeiro com a reconstrução estética, pelo cirurgião plástico ou pelo próprio otorrinolaringologista, e o segundo a reconstrução funcional, de acordo com o desenvolvimento e aeração da orelha média e pneumatização mastóidea. Isto deve-se a alterações na distensibilidade da pele por formação de tecido cicatriciale dificuldades de mobilização da pele quando a cirurgia estética é feita após a funcional. Nos pacientes com síndrome bilateral deve-se realizar a estimulação auditiva precoce pela via óssea. Avaliar o desenvolvimento da linguagem, além de avaliação e controle das vias aéreas superiores. Neste caso, é indicada cirurgia a partir dos três anos de idade, sendo as principais técnicas cirúrgicas empregadas: Técnica de Patee, Técnica de Wullstein-Zoellner, Técnica de Ombredanne, Técnica de Tato e Técnica de Diamante (12).
Outra preocupação é com a permeabilidade do trato respiratório. As supracitadas malformações por vezes impõe a necessidade de traqueostomias ou ainda, manejos craniomaxilofaciais.
CONCLUSÃO A raridade da Síndrome de Goldenhar e sua heterogeneidade de espectros demonstram o caráter multifatorial desta patologia. Tendo como tríade clássica as alterações oculares, auriculares e vertebrais, apresentam a microssomia hemifacial e as displasias de pavilhão auricular como alterações mais frequentes. Por se tratar, provavelmente, de uma síndrome disgenética multifatorial é necessário o aconselhamento genético e o estudo detalhado da causa em cada indíviduo acometido por esta síndrome, uma vez que, fatores associados como ingestão de drogas durante a gestação, diabetes gestacional, ingestão de álcool durante a gravidez, dentre outros podem ser prevenidos, evitando, na medida do possível, o aparecimento de novos casos.
REFERÊNCIAS BIBLIOGRÁFICAS1. Kalavrezos ND, Bochlogyros PN, Panos G. - Surgical corrections of a pacient with Goldenhar syndrome. Heel Period Stomt Gnathopathoprosopike Cheir, 1990; 5(4):147-50.
2. Gorlin RL. Brachial arch and oro-acral disorders. In: Gorlin JJ, Cohen Jr MM, Hennekam RC, editors. Syndromes of the head and neck. London: Oxford University Press; 2001. p.790-7.
3. Bestlmeyer U, Weeda H, Siegert R, Greiwe Schwinger E. Familial Ocurrence of Oculoauriculovertebral Dysplasia and Franceschetti Syndrome. Hno,1996; 44(8):252-5.
4. Altamar RJ. Sindrome de Goldenhar - a propósito de um caso. An. Otorrinolaringol. Iber Am. 1998; XXV:491-7.
5. Regenbogen L, Godel V, Goya V, Goodman RM. Further evidence for an autosomal dominant form of oculoauriculovertebral dysplasia. Clin.Gen 1982; 21:161-7.
6. Hunt JA, Hobar PC. Common craniofacial anomalles: the facial dysostoses. Plat Reconstr Surg. 2002; 110:1714-25.
7. Gorlin JJ, Cohen MMJr, Levin LS. Syndromes of the Head and Neck. 3rd ed. London: Oxford Univ. Press 1990. Pp. 641-649.
8. Morrison PJ, Mulholland HC, Craig BG, Nevin NC. Cardiovascular abnormalities in the oculo-auriculo-vertebral spectrum (Goldenhar syndrome). Am J Med Genet. 1992 Nov 1;44(4):425-8.
9. Verona LL,Damian NG, Pavarina LP, Ferreira CHF, Melo DG. Síndrome de Goldenhar: relato de um caso com discordância em gêmeas monozigóticas. J Pediatria Vol. 82, Nº1, 2006.
10. Laredo FJ, Braga JMB, Kasinsk SK, Caballero JMP. Síndrome de Goldenhar (displasia óculo-aurículo-vertebral). Folha Med. Bras. 1985; 91:361-4.
11. Araneta MRG, Moore CI, Onley RS, Edmonds LD, Karcher JA, McDonough C, Hiliopoulos KM, Schlangen KM, Gray GC. Goldenhar syndrome among infants born in military hospital to Gulfwar veterans. Teratology1997; 56:244-251.
12. Alonso JM, Tato JM. Tratado de Otorrinolaringologia e broncoesofagica. 4º edição.
13. OMIM. Online Mendelian Inheritance in Man. Hemifacial Microsomia [On line]. Disponível em
http://www.ncbi.nlm.nih.gov/entrez/dispomim.cgi?id=164210. Acessado em 22 de abril de 2007.
14. Lessick M, Vasa R, Israel J. Severe manifestations of oculoauriculovertebral spectrum in a cocaine-exposed infant. J Med Gen1991; 28:803-4.
15. Gorlin RJ, Cohen MM, Levin LS. Branchial arch and oroacral disorders. In: Syndromes of the head and neck. 3ed. New York: Oxford University Press; p.641-8.
16. Johnson K, Fairhust J, Clarke NM. Oculoauriculovertebral spectrum: new manifestations. Pediatr. Radiol. 1994; 25:146-8
17. Regenbogen L, Godel V, Goya V, Godman RM. Further evidence for an autosomal dominant form of oculoauriculovertebral dysplasia. Clin Genet. 1982; 21:161- 7.
18. Brosco KC, Zorzetto NL, Costa AR. Perfil audiologico de indivíduos portadores da síndrome de Goldenhar. Rev. Brás. Otorrinolaringol. 2004; 70(5):645-9.
19. Cotin G, Lacombe H. Malformations du Condut-auditif externe et de láreile moyenne. EMC. 20182-A-10. 1985.
20. Rollnick BR, Kaye CL, Nagatoshi K, Hauck W, Martin AO. Oculoauriculovertebral dysplasia and variants: Phenotypic characteristics of 294 patients. Am. J. Med. Genet. 1993; 26:361-75.
21. Greenword RD et al. Cardiovascular malformations in oculoauriculovertebral dysplasia (Goldenhar syndrome). J. pediatr. 1974; 85:816-8.
22. Castori M, Brancati F, Rinaldi R, Adami L, Mingarelli R, Grammatico P, Dallapiccola B. Antenatal presentation of the oculo-auriculo-vertebral spectrum (OAVS). Am. J. Med. Genet. 140A: 1573-1579, 2006.
23. Ostlere SJ, MacDonald B, Athanasou NA. Mesenchymal chondrsarcoma associated with Goldenhar´s syndrome. Arch. Orthop. Traum. Surg. 1999; 30:120-4.
24. Llano-Rivas I, Gonzalez AA, Castillo V, Reyes R, Carnevale A. Microtia: a clinical and genetic study at the National Institute of Pediatrics in México city. Arch. Méd. Res. 1999; 30:120-4.
25. Schaffer AJ, Hine MK, Levy BM. Tratado de patologia bucal. ed.4.Rio de Janeiro: Interamericana; 1985. p.631.
26. Tramba H, Herman P. Formes cliniques dês OMC non cholesteatoma. Encyclopedie Medico-Chirugicale (Paris- France) 20.095-A-10.1993.
27. Rollnick BR. Oculoauriculovertebral anomaly: variability and causal heterogeneity. Am. J. Méd. Genet. Suppl. 1988; 4:41-53.
28. Francois B, de Paepe A, Matton MT, Clement D. Pulse wave velocity recordings in a family with ecchymotic Ehlers- Danlos syndrome. Int. Angiol. 1986; 5(1):1-5.
1. Mestre em Otorrinolaringologia pela Universidade Federal do Rio de Janeiro e Doutorando em Neurociências pela Universidade Federal do Pará. Professor Assistente da Universidade Federal do Pará e da Universidade do Estado do Pará.
2. Monitor da Disciplina de Otorrinolaringologia da Universidade do Estado do Pará. Aluno do Quinto Ano do Curso de Graduação em Medicina da Universidade do Estado do Pará.
3. Aluna do Quarto Ano do Curso de Graduação em Medicina da Universidade do Estado do Pará.
Instituição: Universidade do Estado do Pará - UEPA.
Endereço para correspondência: Francisco Xavier Palheta Neto
Travessa Barão do Triunfo, 3380 - Apto. 502 - Bairro: Marco - Belém / PA - CEP: 66093-050
Telefone:(91) 3224-6517 / (91) 9116-0508 - Telefax: (91) 3236-0227
E-mail: franciscopalheta@hotmail.com
Este artigo foi submetido no SGP (Sistema de Gestão de Publicações) da R@IO em 23 de janeiro de 2007 . Cod. 215. Artigo aceito em 26 de maio de 2007 .